
Cuándo lees por primera vez un protocolo de un ensayo clínico te quedas con cara de poker … multicéntrico, doble ciego, randomizado de grupos paralelos…
Hoy os cuento un poco más de nuestra jerga, para qué con la información del título puedas ya entender mucho más del estudio.
Comenzamos por el principio. El Título Completo: este debe de aportar toda la información para que al lector le resulte evidente lo que se está investigando. Para alguien que esté haciendo una búsqueda bibliográfica debe de ayudarle a diferenciar si le puede o no aportar información en su búsqueda.
Debe contener:
- Información sobre los participantes.
- Intervención.
- Grupos de comparación.
- Desenlaces.
- Fase.
- Diseño del estudio.
También cada ensayo cuenta con un Título Corto o Acrónimo, que no es más que un resumen del título largo, el cual se usa en los formularios de consentimiento informado, este debe de ser:
- Suficientemente claro para entender de qué trata la investigación.
- El acrónimo debe provenir del título largo.
A continuación os explico la clasificación principal de los ensayos clínicos, para entenderlo mejor.
-Ensayo Clínico (Clinical Trial): Estudio sistemático experimental que se realiza tanto en pacientes como en voluntarios sanos para evaluar la eficacia y/o seguridad de uno o varios procedimientos terapéuticos, diagnósticos u otros, así como para conocer los efectos producidos en el organismo humano (farmacodinamia) y/o su absorción, distribución, metabolismo y excreción (farmacocinética).
Según el Investigador y Centros que intervienen:
-Estudios unicéntricos: Son aquellos estudios realizados por un solo investigador o equipo investigador, en un centro hospitalario o en centros dependientes o tutelados del mismo (extrahospitalarios). Son rápidos y fáciles de realizar, pero en contrapartida, tienen el inconveniente de que al realizarse con un número pequeño de pacientes será muy difícil el demostrar posibles diferencias entre tratamientos.
-Ensayo clínico Multicéntrico (Multicenter Clinical Trial): Ensayo clínico realizado en 2 o más centros con un mismo protocolo y un centro coordinador que se encarga del procesamiento de todos los datos y del análisis de los resultados.
Según su metodología, tenemos los ensayos clínicos controlados o no controlados.
-Ensayos no controlados: aquellos que no comportan una comparación con un grupo control o grupo testigo. Se entiende por “grupo control” aquel conjunto de pacientes que recibe un tratamiento estándar, bien sea: placebo, fármaco ya conocido o simplemente, ninguna intervención, pero que en ningún caso recibe el fármaco en investigación.
–Ensayo clínico controlado (Controlled Clinical Trial): es el que incluye al menos dos grupos de pacientes y/o voluntarios sanos, cuya asignación a un tratamiento experimental o control se realiza al azar, de forma que ni el paciente ni el médico responsable de su selección o tratamiento puedan influir en la asignación a un brazo u otro del tratamiento en investigación. Tanto el periodo de reclutamiento como el de tratamiento y de seguimiento han de tener lugar simultáneamente. En la gran mayoría de los casos es la única forma científicamente válida para evaluar la eficacia y seguridad de una intervención terapéutica.
Dentro de los Ensayos Clínicos Controlados nos encontramos con Ensayos Abiertos (open label) o Cerrados.
–Ensayo Clínico Abierto (Open Clinical Trial): aquí tanto el paciente como el investigador conocen la identidad de los fármacos empleados. Este término debe utilizarse únicamente con esta acepción.
-Ensayo Clínico Cerrado: No se conoce la medicación que está recibiendo el paciente. Si es tratamiento activo o si placebo. Dentro de este tipo podemos diferenciar los tipos de ciego (blinding):
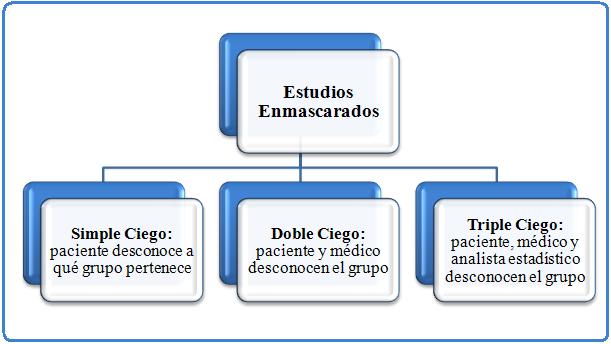
*Simple-Ciego (Single-blind): Se refiere generalmente a que el sujeto desconoce el grupo de tratamiento al que pertenece, aunque es a veces el investigador quien desconoce la asignación de tratamientos. *Doble-Ciego (Double-blind): Tanto el sujeto como el médico desconocen la asignación a los grupos de tratamiento. Dentro de los dobles ciegos tenemos dos procedimientos para mantener ese enmascaramiento de la medicación: Doble simulación (Double-dummy): Procedimiento para mantener el carácter doble-ciego, que consiste en la administración de un placebo de características externas iguales a las de uno o varios tratamientos activos, en situaciones en las cuales la forma de presentación y/o pauta posológica (dosis, vía de administración y frecuencia) sea diferente en el grupo experimental y en el grupo control; y el Enmascaramiento (Blinding, Masking): Serie de medidas (o precauciones) que se toman con el fin de que a lo largo del estudio, bien el paciente, el médico o ambos, desconozcan la asignación de los tratamientos. Incluye randomización ciega, similares características de las muestras e iguales etiquetas. *Triple ciego: donde ni el estadístico conoce el tratamiento recibido por los pacientes. *Evaluación ciega por terceros (Observer-blind): Será cuando se recurre a un tercero, que desconoce el tratamiento que está recibiendo cada paciente, para la valoración de la respuesta. Se utiliza cuando no es posible un diseño doble ciego.
Según el según el diseño del estudio: El diseño del ensayo clínico establece cómo asignar los pacientes a los grupos de tratamiento y las tácticas estadísticas para analizar los datos.
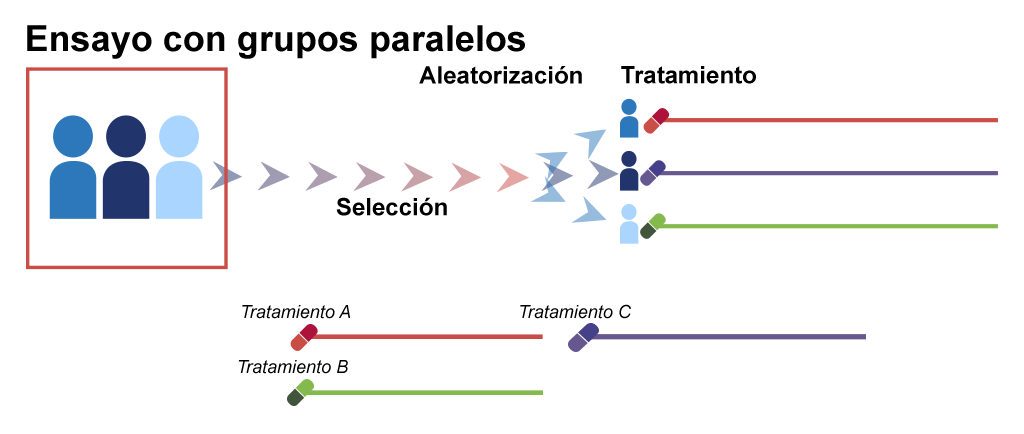
-Ensayo clínico con grupos paralelos (Parallel treatment design): Ensayo clínico en el cual un grupo de pacientes es asignado a recibir el tratamiento experimental, y al mismo tiempo otro grupo recibe el tratamiento control.
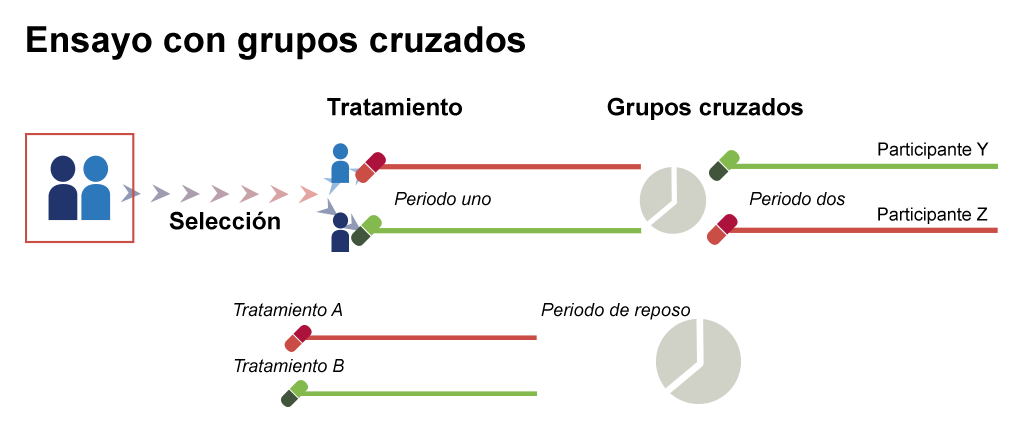
–Ensayo clínico con grupos cruzados (Crossover Clinical Trial): es aquel en el que ambos tratamientos en estudio (experimental y control) son administrados a cada paciente en períodos sucesivos que han sido determinados aleatoriamente, lo que permite a cada sujeto ser su propio control.
-Diseño en parejas (Matched pairs): los sujetos que tienen factores relevantes idénticos se agrupan por parejas (por ejemplo: dos mujeres, rubias, mayores de 30 años y de ojos azules). Si estos datos referentes al sexo, color de pelo, ojos y edad fueron factores relevantes). Uno de los sujetos del par se asigna randomizadamente al grupo del tratamiento activo y el otro sujeto al grupo control o placebo.
-Estudios secuenciales: Son aquellos en los que poniendo a prueba una hipótesis específica, el número de sujetos no está prefijado de antemano sino que depende de los resultados que se van obteniendo a lo largo del mismo.
Según la asignación del tratamiento:
-Asignación Aleatoria o randomización. (Randomization): Procedimiento sistemático y reproducible por el cual los sujetos participantes en un ensayos clínicos son distribuidos al azar en los distintos grupos de tratamiento.

-Ensayos clínicos no randomizados: Son aquellos estudios en los que los pacientes son asignados a uno u otro tratamiento, bien sea siguiendo un método de asignación sistemática predeterminada o el juicio del investigador o del paciente. Se les puede asignar el tratamiento por la fecha de nacimiento (ej.: días de nacimiento impares/días pares = tratamiento nuevo/estándar), la fecha de presentación (ej.: días impares/pares = tratamiento nuevo/tratamiento estándar), la asignación alternada (ej.: pacientes impares/pares = tratamiento nuevo/tratamiento estándar).
Para finalizar nos encontramos con:
-Estudios observacionales: Estudio epidemiológico analítico en el que el investigador no determina la asignación de los sujetos a cada grupo, sino que se limita a registrar (observar) lo que ocurre en la realidad, en la práctica clínica habitual. Se trata de ‘comprobar’ en pacientes reales, que están en tratamiento, que efectivamente los resultados obtenidos también se dan en el día a día médico.
Por último, haceros un pequeño recordatorio de las fases de un ensayo clínico.
-Ensayo clínico fase I (Phase I Clinical Trial): Constituye el primer paso en la investigación de un fármaco nuevo en el hombre, a partir de los cuales se generará la información preliminar sobre el efecto y la seguridad del mismo en sujetos sanos y a veces en pacientes (antineoplásicos). Incluye estudios de farmacocinética y farmacodinamia.
-Ensayo clínico fase II (Phase II Clinical Trial): Representa el segundo estadio en la evaluación de un nuevo fármaco en el ser humano. Se realiza en pacientes que padecen la enfermedad o la entidad clínica de interés. El principal objetivo de los ensayos clínicos en esta fase es proporcionar información preliminar sobre la eficacia del fármaco y suplementar los datos de seguridad obtenidos en la Fase I. Por lo general, aunque no en todos los casos, los ensayos clínicos realizados son controlados con asignación aleatoria al tratamiento.
-Ensayo clínico fase III (Phase III Clinical Trial): Conjunto de EC destinados a evaluar la eficacia y seguridad del tratamiento experimental en la indicación estudiada, considerando las alternativas disponibles. Estos estudios constituyen el soporte para la autorización del registro y comercialización de un fármaco a una dosis y para una indicación determinada, por ello deben ser controlados y randomizados, y a ser posible de carácter doble ciego, e incluir un número suficientemente elevado de pacientes que permita demostrar la eficacia y seguridad comparativa entre los tratamientos en estudio.
-Ensayo clínico fase IV: (Phase IV Clinical Trial): Comprende los ensayos clínicos que se realizan después de la comercialización de un fármaco. Estos podrán ser ensayos similares a los descritos en fase I, II y III si estudian algún tipo de efecto aún no valorado, por ejemplo para una nueva indicación, o bien los específicamente fase IV, incluidos en un programa de farmacovigilancia, que deberán ser también controlados, randomizados, y prolongados en el tiempo para evaluar eficacia y/o seguridad a largo plazo.
Os pongo algunos ejemplos para que lo entendáis.
- Estudio de fase III, multicéntrico, aleatorizado, doble ciego, controlado con placebo y un comparador activo para evaluar la eficacia y seguridad de XXX en pacientes con XXX de moderada a grave.
- Ensayo en Fase III, aleatorizado, abierto, multicéntrico para evaluar la eficacia de XXX subcutáneo después de doce semanas de tratamiento y evaluar la seguridad, tolerabilidad y eficacia a largo plazo en pacientes de X años a menos de X años de edad con XXX crónica de moderada a grave.
- Estudio de Fase IIb aleatorizado, con doble enmascaramiento, controlado con placebo y con dosis múltiples para demostrar la seguridad y la eficacia de XXX en sujetos con XXX activa.
- Ensayo en Fase III. Aleatorizado, doble ciego de grupos paralelos, controlado con placebo para evaluar la eficacia y seguridad de XXX, en pacientes con XXX de moderada a grave.
Podéis encontrar muchas mas info en:
https://www.sefh.es/bibliotecavirtual/fhtomo1/cap24.pdf
Esta vez se me ha ido un poco de las manos escribiendo, pero creo que es interesante, para quienes os estéis iniciando en esta profesión, establecer unos buenos cimientos para la construcción de vuestra carrera profesional.
Nos vemos pronto, aquí seguimos en verano!
Un comentario en “Seguimos aprendiendo.”